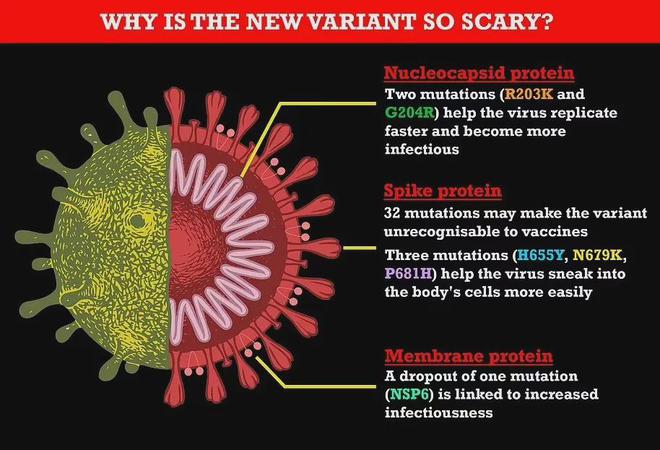
从本周逆转录病毒和机会性感染大会上得到信息,用于高效新冠疫苗的信使RNA (mRNA)也有希望在预防艾滋病方面取得成果。这些疫苗由美国辉瑞生物技术公司(fizer-BioNTech)和莫德纳(Moderna )生产。
尽管经过了30多年的研究,但科学家们在研制预防艾滋病毒疫苗方面几乎没有取得成功。迄今为止,只有一种疫苗方案——金丝雀痘载体引物和gp120蛋白助推器——在人类研究中证明了部分保护作用;但在最近的一项大型试验中却被证明无效。另外两项大型研究——Mosaico和Imbokodo——目前正在测试一种方法,它使用腺病毒引物,和一种包含多种艾滋病毒毒株的蛋白质“组合体(马赛克)”助推器。
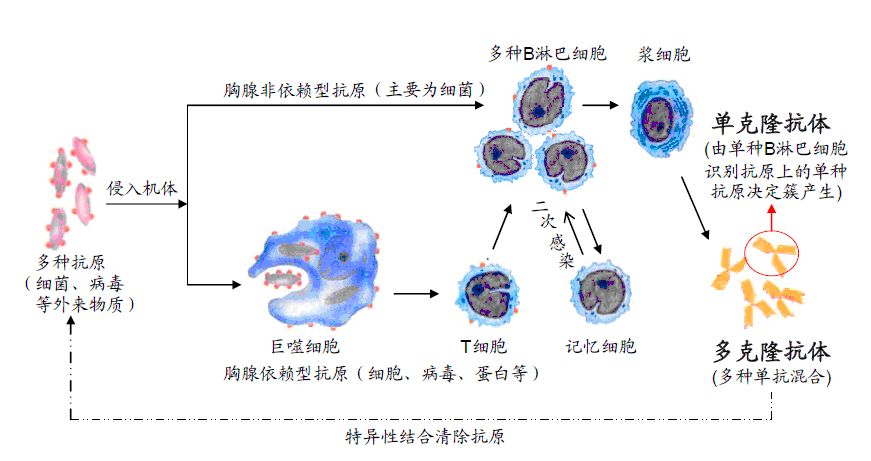
美国国家过敏症和传染病研究所(NIAID)的张鹏博士(Dr Peng Zhang )及其同事正在与莫德纳合作,采用一种不同的方法,即使用脂质纳米颗粒或脂肪泡,传递一小段核酸,从而为制造蛋白质提供指令。信使RNA存在于整个细胞中,起信使作用,因此得名。
它们不构成基因组的一部分,也不构成生命的基本蓝图。基因组以类似但更稳定的分子DNA形式存在于细胞核中。
研究人员设计了一种疫苗方案,将mRNA引入细胞,并指示其制造艾滋病毒三种不同亚型的外层包膜蛋白,以及来自SIV (猿猴免疫缺损病毒)的结构gag蛋白。然后这些细胞组装这些蛋白质,制造类病毒颗粒艾滋病毒,引发免疫反应。这些颗粒不是病毒,因为它们自身没有遗传物质,不能繁殖——但它们对免疫系统来说看起来像病毒。
在这项研究中,7只雄性猕猴接受了两种疫苗方案中的一种,而另外7只接受安慰剂注射。在20周的时间里,所有猕猴先被注射三次一种含有艾滋病毒B亚型包膜蛋白mRNA的疫苗,这是欧洲和北美的主要病毒类型。此外,有三只猕猴也接受了含有稳定HIV刺突蛋白的最终助推器,称为SOSIP三聚体艾滋病毒,它将蛋白质保持在开放的形状,暴露出一个更容易被广泛中和抗体识别的保护区。
在接受完整的疫苗方案后,猕猴们在13周中将直肠暴露于一种二级SHIV病毒,这是一种经过工程改造的HIV/SIV混合病毒。
一级病毒具有更开放的包膜三聚体形状,更容易被中和抗体识别,而二级和三级病毒具有更封闭的形状,对这些抗体有中度或低度的敏感性。大多数流行的艾滋病毒毒株被归类为二级毒株。
接种疫苗的猕猴迅速产生了与蛋白质三聚体结合的高水平抗体,并且中和了针对B型艾滋病病毒蛋白的抗体——第一组疫苗中的抗体。从49周左右开始,他们产生了较低水平的对抗A亚型和C亚型蛋白质的交叉反应中和抗体。
在免疫方案结束时,猕猴已产生了针对一系列病毒毒株的广谱二级中和抗体。
在第二轮暴露后,安慰剂组的所有7只猕猴都在大约一个半月内被感染。
所有接种过疫苗的猕猴在第一个月左右都没有感染,但随后开始感染。然而,有些猕猴在所有暴露结束后的两个月仍未感染。
结果表明,总的感染风险降低了85%,只接受mRNA疫苗而没有增强剂的猕猴降低了76%,而那些接受mRNA疫苗加三聚体蛋白增强剂的猕猴降低了88%。这种保护作用与CD4结合部位的抗体存在有关,HIV和SIV用CD4结合部位来进入细胞。
张博士说:“mRNA平台在未来开发艾滋病毒疫苗方面非常有前途。”“简单来说,即mRNA疫苗结合稳定蛋白助推器能够打开CD4结合部位,”理查德·布普(Richard Koup)博士说,他是美国国家过敏症和传染病研究所疫苗研究中心的研究人员。
最终,猕猴“产生了正确的中和活动,部分免受感染,” 张博士补充说。“这为人类疫苗接种提供了新的途径。”
/uploads/",@me) /}