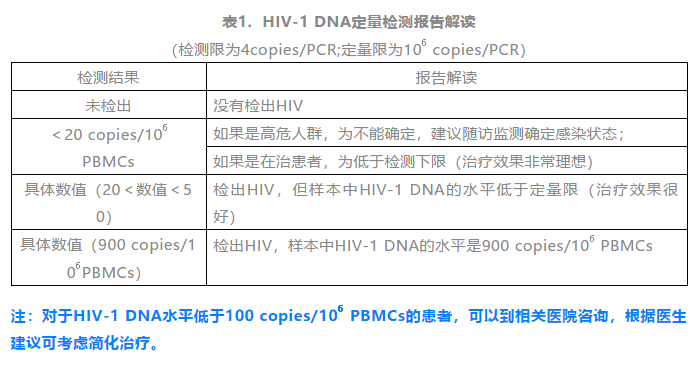
前言
抗逆转录病毒治疗(antiretroviral therapy, ART)虽然能有效抑制HIV病毒,但不能根治艾滋病(AIDS)。AIDS功能性治愈要求停止ART后患者体内HIV-1 RNA长期低于检测下限,而且CD4+T淋巴细胞数量和机体免疫功能保持正常。这一直是全球研究热点和难点。近年来,AIDS功能性治愈在HIV-1储存库激活和清除、免疫治疗、干细胞移植、基因编辑等方面的临床试验取得了长足进步。
1.HIV-1病毒储存库的激活和清除
该原理为使用潜伏再激活药物(LRAs)激活潜伏HIV-1,免疫监视系统通过细胞毒性T淋巴细胞反应或抗体依赖性细胞介导的细胞毒作用,识别和清除表达HIV-1的细胞将其杀灭,加速病毒储存库的消除。但目前尚无明确有效的LRAs。
组蛋白去乙酰化酶抑制剂代表药物伏立诺他(SAHA)、罗米地辛(RMD)和帕比司他(PNB)均已进入II期临床试验,证实能够有效激活潜伏HIV-1,但进入II期临床试验后效果并不理想。
西达本胺、三氧化二砷在动物试验中能有效激活储存库中的病毒,目前正在进行临床研究。
蛋白酶C(PKC)激动剂能激活PKC信号通路引起核因子κb和激活蛋白1活化,从而激活潜伏HIV-1。
目前对小分子PKC激动剂,例如:苔藓抑素、炔诺醇B。其中炔诺醇B毒性小,潜伏激活的作用较强。TLR7激动剂GS-9620能够激活猴子体内的CD4+T淋巴细胞和NK细胞,同时还能激活潜伏的病毒,但仍未予临床应用证实。
伊克昔佐米被证明可以诱导患者来源的CD4+T淋巴细胞凋亡,并在体外条件下降低病毒DNA载量,被认为是减少感染细胞数量的有效候选药物,目前正在进行I期临床试验。
2.免疫治疗
免疫治疗包括免疫细胞回输、广谱中和抗体及治疗性疫苗等,可以单独使用来消除病毒储存库,也可以与LRAs合用,先激活潜伏HIV-1再杀灭。
①嵌合抗原受体(CAR)T细胞是表达CAR的工程T细胞,用于识别和杀死靶细胞。第二代CAR-T研究表明,在感染HIV-1的人类小鼠和感染SHIV的猪尾猕猴中,采用慢病毒介导的自体CD34+T淋巴细胞转导过继转移疗法可以获得比较满意的疗效,CAR可以安全地植入骨髓,顺利成熟并成为整体身体的功能性免疫细胞。目前在ClinicalTrials.gov网站上注册的针对HIV-1的CAR-T细胞疗法临床试验极少,目前登记在册开展招募受试者的仅有2项,具体疗效未见报道。
②针对CD4+T淋巴细胞经典结合位点的广谱中和抗体VRC01、3BNC117完成了1期临床研究,证实其在感染及未感染人群中均具有良好耐受性,且3BNC117还展现了良好的体内抗病毒活性。2018年Emu等探索了CD4特异性抗体ibalizumab联合抗病毒治疗在多重耐药HIV-1感染者中具有较好治疗效果(Ⅲ期)。但有研究发现,单独使用ibalizumab时可能耐药性逐渐增加。近期Wang等的UB-421 II期临床研究发现,该单药用于长期抗病毒治疗控制良好的患者停药后转换,在研究期内均维持了良好病毒学应答,CD4+T淋巴细胞计数稳定,但极有可能也存在耐药风险。
③迄今为止,已有六种HIV-1疫苗的概念应用于人体,评估其有效性。两项VAX003、DNA/rAD5临床2b试验,没有显示出疗效。RV144疫苗有约30%的效力,接种疫苗不影响HIV感染者的病毒载量CD4+计数,保护效果温和。
综合目前研究结果,单一的免疫治疗方式疗效仍欠佳,甚至出现耐药可能,联合应用看似短期内可获得良好效果,但长期疗效不明朗。
3.干细胞移植
干细胞移植是通过对AIDS患者进行造血干细胞移植(HSCT),以期供体的干细胞持续产生正常T淋巴细胞,而移植物抗宿主反应可能有助于清除病毒储存库。
著名的“伦敦病人”是接受了CCR5△32纯合子突变供体的骨髓干细胞移植,不仅治愈了淋巴瘤,还在停止ART后HIV-1病毒抑制仍持续存在。根据报道,该例“伦敦病人”是继“柏林病人”以后观察到的持续时间最长的HIV缓解:外周血HIV-1 RNA低于检测下限,HIV-1 DNA水平迅速下降;Western blot显示CD4+T淋巴细胞 不表达CCR5,体外检测显示CD4+T淋巴细胞对CCR5嗜性毒株型的HIV-1抵抗,但对CXCR4嗜性毒株型的HIV-1仍然敏感;移植后的HIV-1特异性抗体Western blot阳性,p24/p31带缺失,HIV-1特异性抗体亲和力下降到与“柏林病人”移植后相当的水平。然而,该患者的AIDS是否得到根治,仍需进一步以观其效。
尽管HSCT治疗AIDS取得了不俗成绩,但其推广存在极大困难。首先,由于移植的成本高、风险大,该策略前提需要HIV-1感染者合并血液病,才值得进行骨髓移植;其次治愈艾滋病,骨髓的供者不仅要具有相应的基因缺失,还需要与受者的配型匹配,同时符合两个条件的几率非常低,而在我国,具有CCR5Δ32纯合子突变基因者极为罕见。如果能解决上述困难,HSCT必然是极具前景的一种策略。
4.基因编辑
基因编辑技术的飞快发展,使其成为AIDS功能性治愈的重要手段。目前AIDS基因治疗研究多集中于体外或非人灵长类,人体试验极少。
最近Xu等报道了世界上首次通过基因编辑技术敲除人体造血干细胞CCR5基因,并回输给患有急性淋巴细胞白血病的AIDS患者的研究。该研究利用前期优化的CRISPR/Cas9基因编辑造血干细胞技术,在供者来源的CD34+造血干细胞上实现了17.8%的CCR5基因敲除效率。患者的白血病在移植后19个月随访中处于完全缓解状态,而且供者型细胞完全嵌合,骨髓细胞基因组持续检测到CCR5基因编辑。通过对患者移植后多个骨髓样本的全基因组分析,并未发现基因编辑的脱靶效应和相关副作用。该研究显示,患者停止ART后4周治愈艾滋病,外周血HIV- 1 RNA载量从检测不到反弹到3×107拷贝/毫升,但移植19个月后,检测外周血样本发现HIV-1病毒噬性并没有发生改变(依然为CCR5噬性)。
该研究为进一步完善利用基因编辑技术和治愈AIDS提供了重要参考和指导。但在基因编辑研究中,特别需要注意伦理问题。
总结
“柏林病人”和“伦敦病人”的实例说明,AIDS功能性治愈并不是遥不可及。尽管攻克AIDS的道路任重道远,但相信不远的未来必将获得革命性突破。
/uploads/",@me) /}