公司概况 »公司新闻 »艾滋病毒研究进展简述
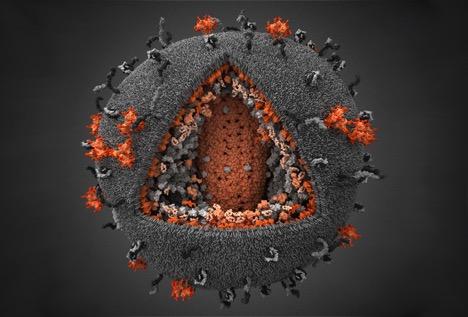
艾滋病毒研究进展简述
距离1981年美国首次报告人类免疫缺陷病毒(HIV)感染导致获得性免疫缺陷综合症(艾滋病)已有将近40年。自那时起,该领域的很多科学家们潜心专研,努力寻找预防和治疗的方法, 甚至也有关于治愈艾滋病患者的报道。在私人和政府机构的支持下,每年都花费数百万美元来支持这项研究。以美国为例, 2018年和2019年通过美国国立卫生研究院(NIH)分别调配了26,945.4百万美元和28,021.4百万美元来支持相关的研究;此外,美国总统艾滋病紧急救援计划(U.S. President’s Emergency Plan for AIDS Relief, PEPFAR)也为全球艾滋相关的调查等事宜提供资金支持。
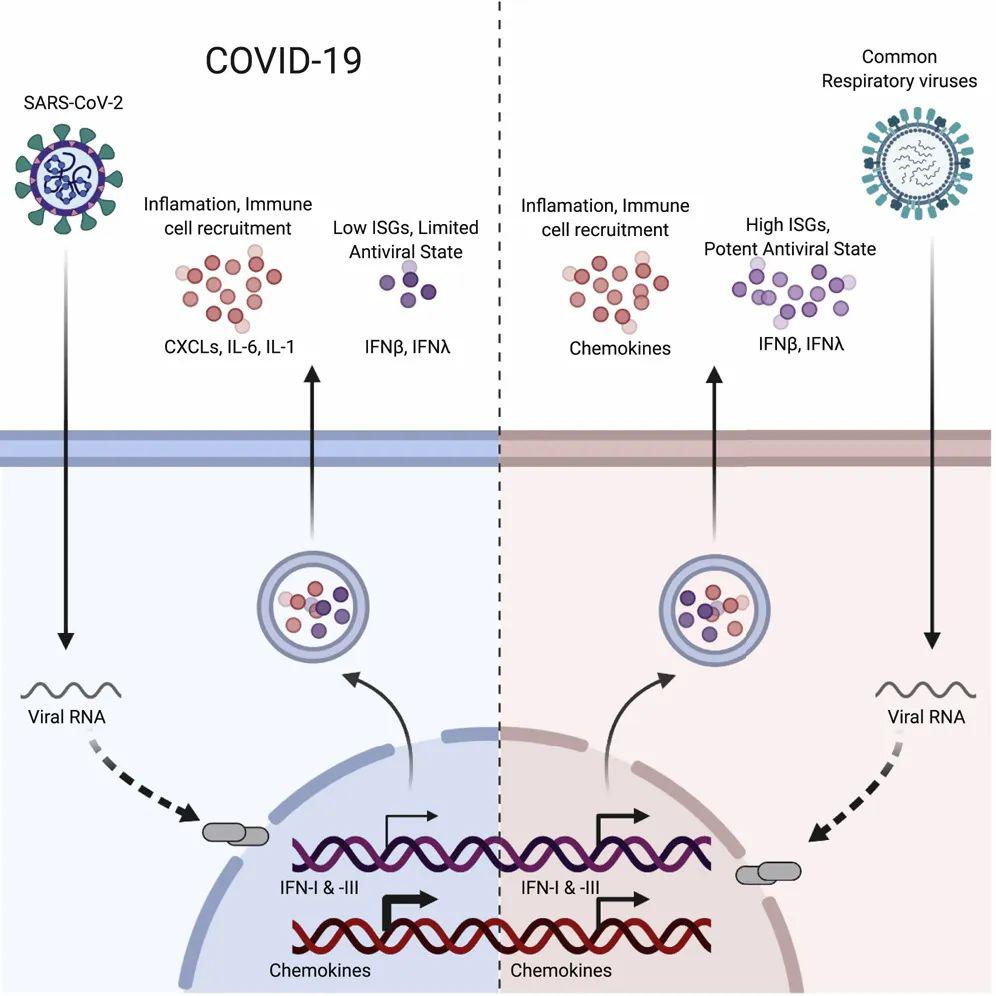
近年来,有些报道称,通过一些新的治疗方法,患者体内的病毒水平能在一定时间内控制在的安全范围内;本篇中将回顾近年来最突出的成就,并对相关发现是否能被开发成有用的治疗工具做初步探讨。
艾滋病毒研究的关键里程碑a. 柏林病人(Hütter, et al., 2009)
第一个AID治愈的患者Timothy Ray Brown是艾滋病病毒阳性,他同时患有急性髓性白血病。1995年被诊断出艾滋病后,他不得不从家乡美国华盛顿州的西雅图搬到了德国柏林。多年来,他一直靠服用了抗逆转录病毒药物来控制艾滋病毒感染。但是,在2006年,他不幸患上了急性髓性白血病。一年后,在经历了两次不成功的诱导化疗和一次巩固化疗后,他在柏林接受了两次骨髓干细胞移植手术;很幸运的是,他的病情得到了有效的治疗,艾滋病毒感染更是被鉴定为“功能性治愈”。原来,骨髓供体具有罕见的基因突变,即CCR5 Δ32突变,该突变可以防止大多数HIV病毒株感染白细胞;因为HIV需要与共受体CCR5或CXCR4结合,从而进入细胞。在Tim接受移植手术近20个月后,也就是2008年,Gero Hütter博士在美国波士顿举行的CROI会议上公开宣布这一成功治疗的消息。直到今天,Tim体内的病毒依然控制在无法被检测到的范围之内,他的案例给很多艾滋患者带去治愈的希望。
b. 伦敦病人(Gupta, et al., 2019)
2019年3月初,一份关于匿名“伦敦病人”的突破性成果在Nature杂质发表。该患者是一名成年男性, 2003年感染HIV-1,而后于2012年末被诊断患有霍奇金淋巴瘤。与柏林病人相似,伦敦病人于2016年接受了CCR5Δ32/Δ32造血干细胞移植,并在移植16个月后停止服用抗逆转录病毒疗法。当时研究人员披露这项研究时,患者已停止抗病毒治疗18个月。事实上,该患者经历了两轮基于纯合CCR5Δ32/Δ32供体细胞的同种异体造血干细胞移植(allogeneic haematopoietic stem-cell transplantation , allo-HSCT),并伴以轻度化疗;而不是像柏林病人那样,一轮移植和严格的全身照射。该研究表明,表明单个allo-HSCT治疗可能足以实现HIV-1缓解。
c. 抗HIV广泛中和抗体(Mendoza, et al., 2018)
在过去的几十年中,抗体为疾病的治疗带来了革命性的改变;在艾滋病的治疗方案中,单克隆抗体也对广泛的HIV分离株具有强大的中和活性。其中,对大多数HIV分离株具有高中和活性的那些被命名为广泛中和抗体(Broadly Neutralizing Antibodies, bNAbs),并且已被用于设计抗HIV疫苗。虽然bNAbs作为抗逆转录病毒药物的潜在替代品上具有很大的潜力,但许多临床研究的结果表明HIV可以对bNAbs治疗产生抗药性。然而,在2018年,Mendoza等报道,在参加1b期临床试验的9名患者中hiv病毒,两个bNAb(3BNC117和10-1074的组合)组合的治疗方案下,三轮给药带来病毒抑制的时间能达到15周,甚至超30周(中位数为21周)。该发现引发了一系列关于组合bNAb治疗的临床试验。
d. 迈阿密猴(Martinez-Navio, et al., 2019)
通过抗体输注可以不同程度地抑制病毒复制,但艾滋病人仍需要重复输注以维持体内的抗体浓度。使用腺相关病毒(AAV)进行基因转移有望实现单次给予AAV载体承载单克隆抗体后实现长期的病毒抑制, 即“功能性治愈“。腺相关病毒(AAV)是一种无害高效载体;使用腺相关AAV病毒载体一旦感染细胞,就可以使细胞无限地生成病毒载体中承载的基因所表达的蛋白。Desrosiers博士领导的一项研究最近报道了通过在恒河猴中使用腺病毒辅助病毒(AAV)编码的单克隆抗体进行HIV预防和治疗的进展。四只HIV感染的恒河猴的三联mAb处理86周的结果显示,一只猴子的病毒载量在三年内维持了无法检测的水平。进一步的研究在另外12只猴子的身上进行:他们将猴子分成了两大组,使用承载了四种mAb的AAV递送的“quad group”和使用承载了两种mAb的AAV递送的“bigroup”。结果表明,来自quad group的两只猴子的病毒抑制控制在合理水平之内。这两项研究的结果为AAV递送抗HIV mAb疗法提供了概念证据,给实现AIDS患者的功能性治愈带去了更多的证据和希望。此外,本研究强调了进一步了解抗药物抗体(anti-drug antibody, ADA)对未来在人体中应用新方法至关重要。
为功能性治愈消除障碍
尽管柏林病人和伦敦病人幸运地通过干细胞疗法实现了功能性治愈;并且组合bNAb免疫疗法具有很大的前景。但是,这些方法实现在临床中的常规应用仍然存在若干挑战。
首先,干细胞治疗由于医学并发症而具有高风险,例如移植物抗宿主病(Graft-versus-host disease, GvHD)。接受者需要服用免疫抑制药物,此类药物的使用使得患者更容易受到细菌和病毒感染。另一方面,为了确保移植的成功性,通过匹配供体细胞和受体细胞的表面分子来监测自我识别是至关重要的,这对常规临床应用构成另一个障碍。此外,由CCR5突变诱导的HIV耐受性可允许病毒使用CXCR4受体,因此增加CCR5缺陷型基因型被HIV感染的可能性。
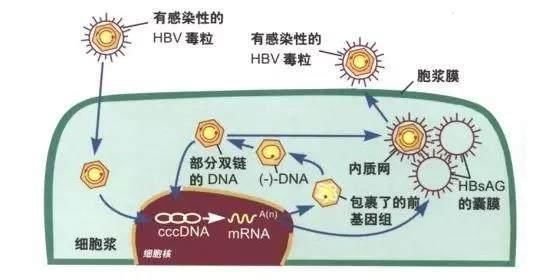
另外,对HIV-1进入CD4 +细胞至关重要的包膜糖蛋白GP120的氨基酸序列变化很快。其带来的序列多样性将通过与CXCR4而不是CCR5结合而引发病毒的进化,并因此增加HIV-1预防和治疗策略的复杂性。同时,HIV-1作为高度多样化的病毒,对bNAbs具有不同程度的敏感性,以及接受免疫治疗的患者中病毒存量的差异hiv病毒,都对组合bNAbs患者的治疗提出了挑战。急切需要解决这些障碍的创造性方法以确保这些新型治疗方法在所有诊所中得到有效和普遍的应用。
金斯瑞在HIV研究上的支持
GenScript已向全球科学界提供了多达100万个基因合成项目,这些项目已经帮助科学家们完成了许多里程碑式的成就,例如Feng Zhang的CRIPSR基因组编辑、国家过敏研究所疫苗研究中心(VRC)开发的新型HIV疫苗。在这一“迈阿密猴”艾滋病治愈的进展中,所报道的含有mAb编码序列的AAV载体构建体的设计、优化和合成由金斯瑞完成。我们非常荣幸我们的基因合成和克隆帮助了Desrosiers博士的研究,并期待能够为更多的客户提供高质量的基因等服务和产品来推动科学研究及医药研发进程。
客户评价
"GenScript provides excellent services in a variety of research needs. I have been using GenScript services for over 10 years now, and the products and services provided have been to my highest satisfaction, and that at blazing speed and reasonable costs. I mostly used GenScript's molecular biology services, but also protein analysis and expression services. Our regional customer support specialist has provided exceptional help and superb assistance. Thank you GenScript for making our research faster and smoother."
- Dr. Sebastian P. Fuchs, University of Miami – Miller School of Medicine
"GenScript delivers excellent quality and reliability in DNA synthesis and cloning services at a very competitive price. Generating our constructs with them saved us plenty of time and headaches. Moreover, they flawlessly adapt to our specific needs on every occasion, and the customer experience is always superb."
- Dr. Jose Martinez-Navio, University of Miami – Miller School of Medicine
相关文献Gupta, et al. (2019) HIV-1 remission following CCR5Δ32/Δ32 haematopoietic stem-cell transplantation. Nature. doi: 10.1038/s41586-019-1027-4Hütter, et al. (2009) Long-Term Control of HIV by CCR5 Delta32/Delta32 Stem-Cell Transplantation. N Engl J Med, 360: 692-698Martinez-Navio, et al. (2019) Adeno-Associated Virus Delivery of Anti-HIV Monoclonal Antibodies Can Drive Long-Term Virologic Suppression. Immunity 50: 567-575Mendoza, et al. (2018) Combination therapy with anti-HIV-1 antibodies maintains viral suppression. Nature 568: 479-484
/uploads/",@me) /}