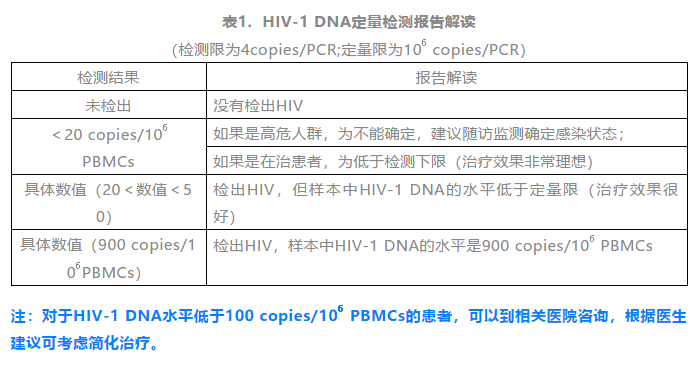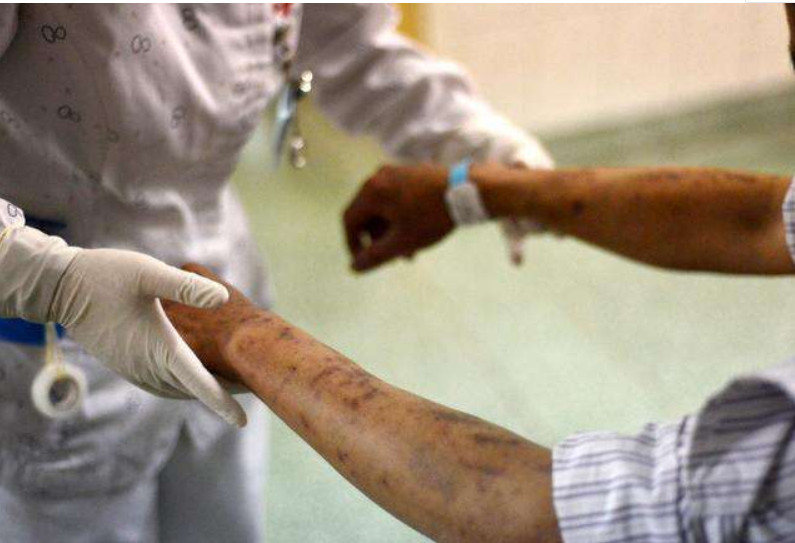
艾滋病(AIDS)是一种由人类免疫缺陷病毒(HIV)引起的、危害性极大的传染病。一旦不幸感染了HIV,人体免疫系统将遭受严重破坏hiv病毒,进而引发各种临床症状。更可怕的是,直至目前,艾滋病仍没有疫苗和特效药。
据联合国艾滋病规划署数据,全球范围内HIV携带者和艾滋病患者人数从2013年末的3430万人增至2018年末的3800万人,且数量仍在逐年增长。与此同时,国家卫健委指出,中国每年大约新增8万例艾滋病,其中高达3000例是青年学生。
由此看来,中国乃至世界的艾滋病流行形势不容乐观,因此,探究艾滋病的复制周期并以此开发新的治疗途径是十分迫切和重要的。
近日,美国犹他大学和弗吉尼亚大学的研究人员在国际顶尖学术期刊 Science 上发表题为:Reconstitution and visualization of HIV-1 capsid-dependent replication and integration in vitro 的研究论文。
这项研究实现了数十年来的梦想——体外重构了感染HIV的第一步。具体而言,研究人员通过冷冻电镜和分子模型重构监测HIV病毒基因组复制和整合过程,这一研究进展使人类对HIV生命周期的早期阶段有了新的认识,并推动相关药物和治疗途径的开发。

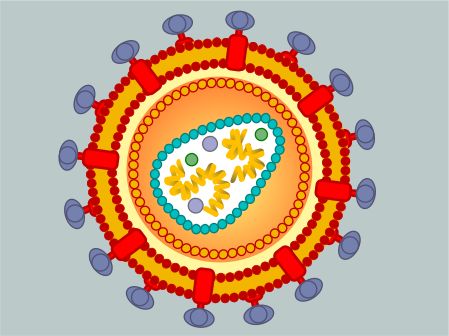
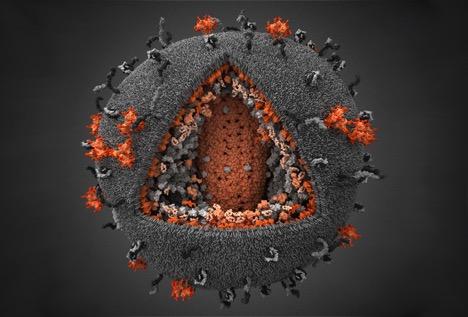
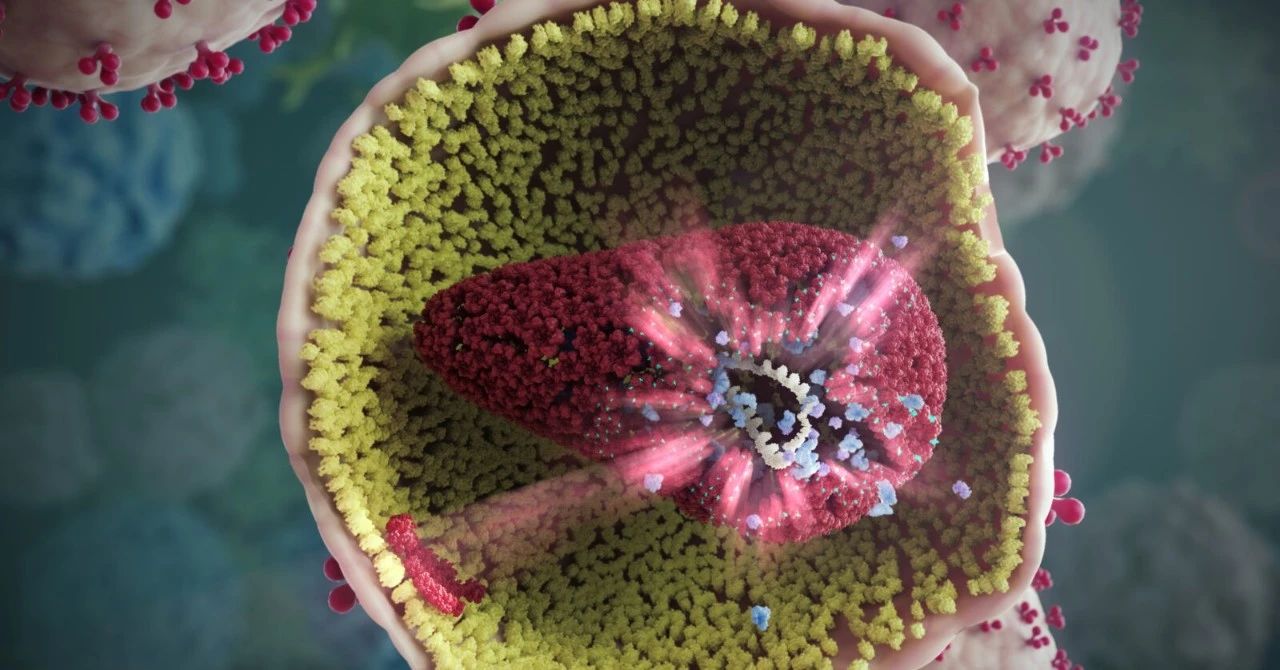
实际上,尽管艾滋病毒很危险,但它的外表却十分简单——这种病毒就像一个圆形的冰淇淋蛋卷,由外面的蛋白衣壳(Capsid)包裹着内部的病毒核酸。在此之前,科学界普遍认为病毒衣壳主要功能是保护内部脆弱的遗传物质。
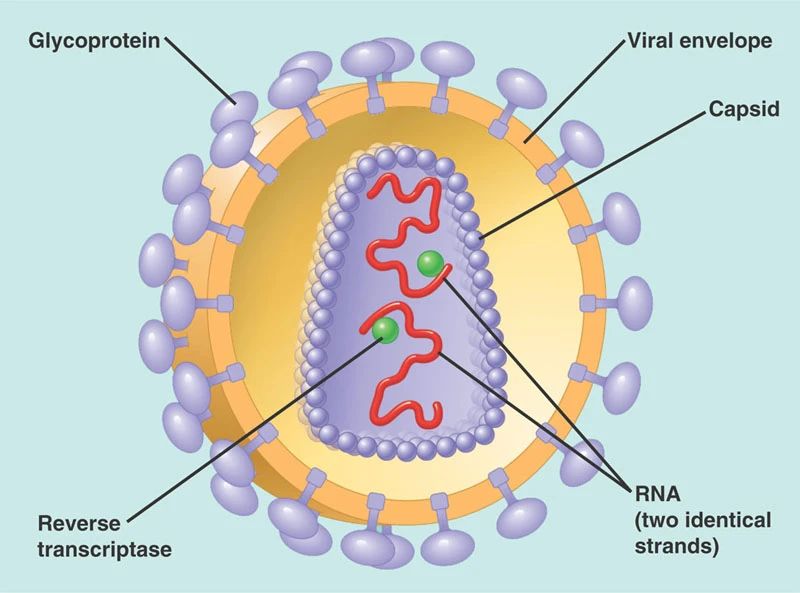
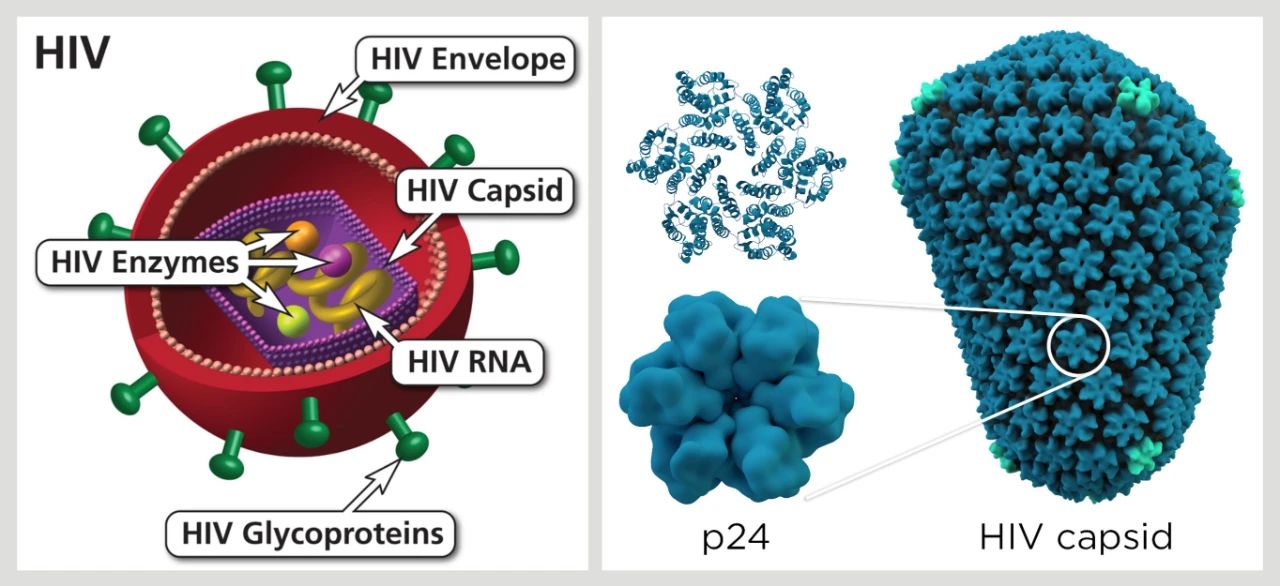
然而,如今这项研究却表明,HIV衣壳蛋白在病毒感染过程中也扮演着积极的角色。
在本研究中,研究团队通过无细胞系统模拟重构了HIV感染的最初步骤,从而以前所未有的方式实现对HIV病毒的精确控制。他们发现,当他们使用遗传和生化方法来破坏衣壳的稳定性时,HIV病毒将无法有效复制其遗传物质。
值得一提的是,这是第一次直接证明,HIV的病毒衣壳不仅仅是一种包装结构hiv病毒,它本身也是艾滋病毒感染过程的一个重要组成部分。
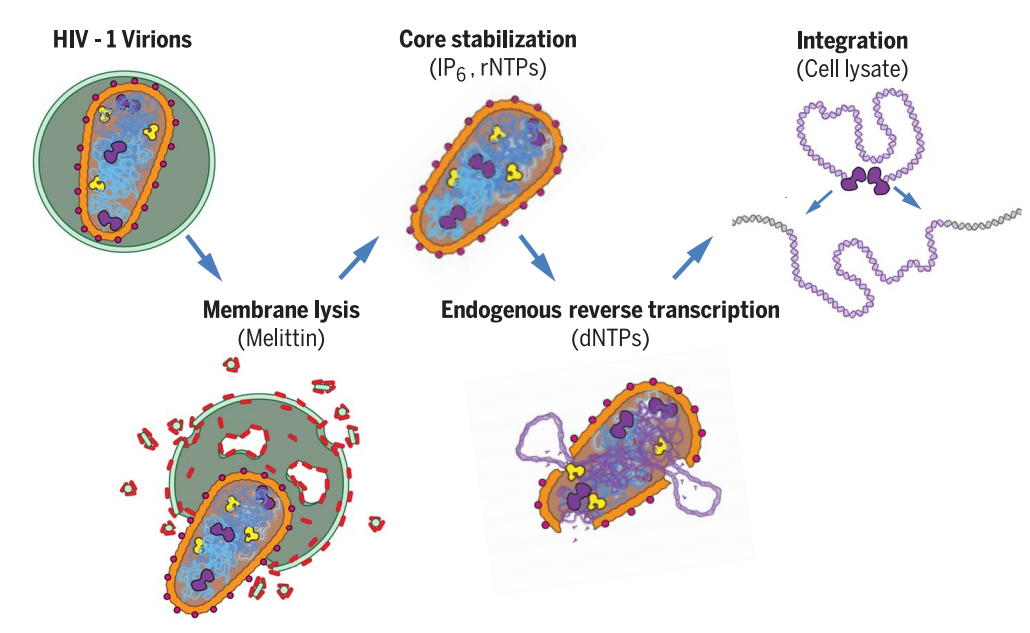
病毒衣壳依赖的HIV-1复制和整合过程
正所谓“眼见为实”,为了增强研究结论的说服力,研究人员还通过冷冻电子断层扫描(cryo ET)和分子模型重构技术直接观察到HIV病毒的衣壳蛋白。研究小组将240个微小的衣壳蛋白亚基可视化,这些亚基拼在一起形成了圆锥形的外壳。
事实上,为了感染宿主细胞,HIV必须将其单链RNA基因组逆转录为双链DNA副本,并将该副本整合到宿主染色体中。而通过电镜观察,研究人员发现,HIV的病毒衣壳在整个逆转录复制过程中基本保持完整。
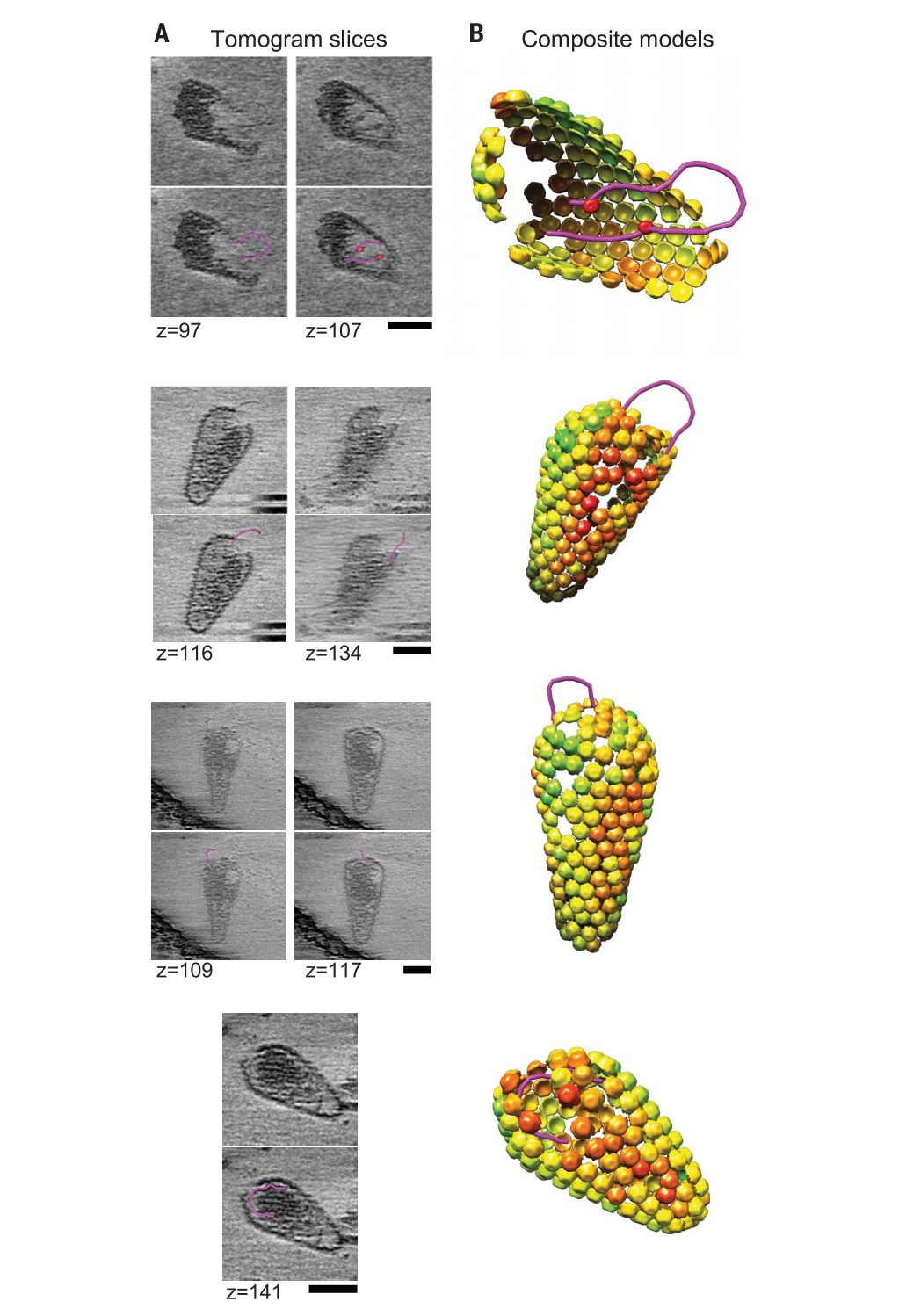
病毒复制过程中核心颗粒的冷冻电子断层扫描和分子模型重构
文章的通讯作者、犹他州大学的 Wesley Sundquist 教授说道:“这和教科书上说的不一样,研究数据表明,HIV的病毒衣壳在支持高效逆转录方面发挥着积极和不可或缺的作用。”
有趣的是,此前吉利德公司开发了一种艾滋病药物——GS-CA1,该抑制剂的靶点恰好是HIV的病毒衣壳,并在Ⅰ期临床试验中表现良好,但具体的作用机理却一直得不到解释。如今,这项研究成果对这一药物作出了理论支持,并有望进一步改进该类药物的设计。
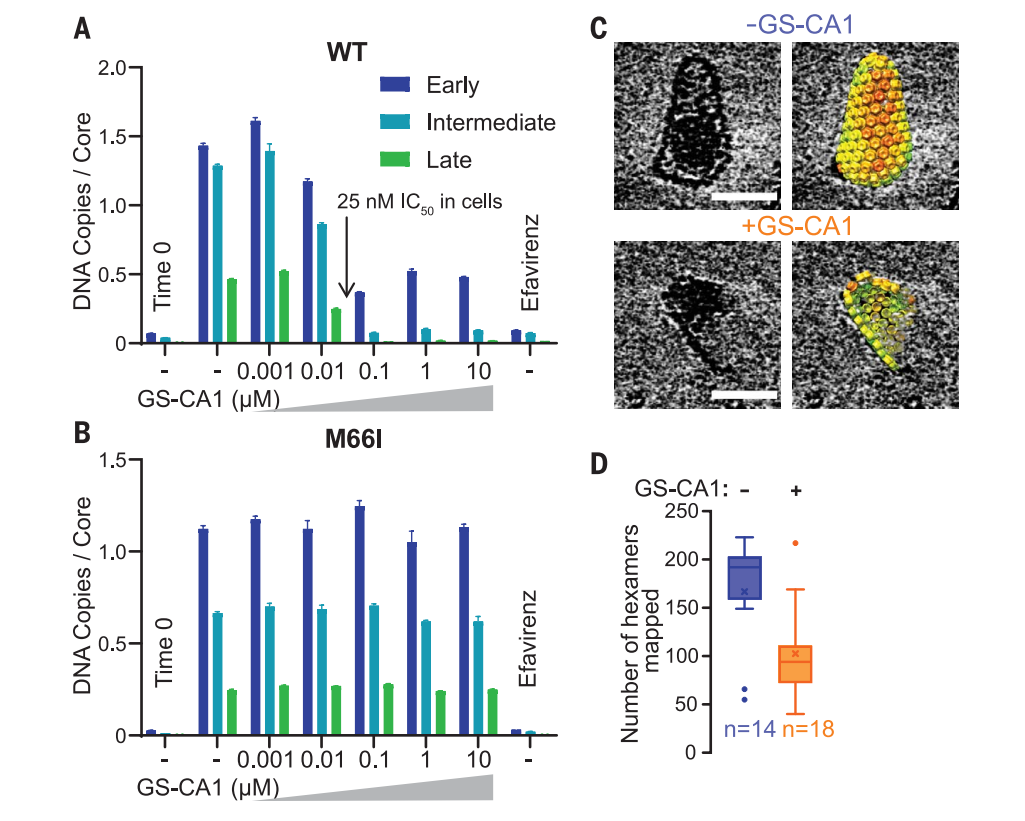
衣壳抑制剂GS-CA1的作用效果
文章的共同第一作者Pornillos说道:“这项研究不仅完善了HIV感染过程的基础知识,还在转录和翻译方面帮助我们找到更好的、阻止HIV的方法,这就是为什么它是伟大的研究!”
总而言之,本研究表明,HIV的病毒衣壳在病毒的逆转录过程中起着积极而不可或缺的作用。因此,研究团队认为整个病毒核心颗粒——包括衣壳,才是真正的病毒复制复合体。除此之外,衣壳在保护病毒基因组免受先天免疫传感器监视、帮助核心颗粒穿过细胞质、进入细胞核和进入整合位点等方面也扮演着重要的角色。
论文链接:
/uploads/",@me) /}