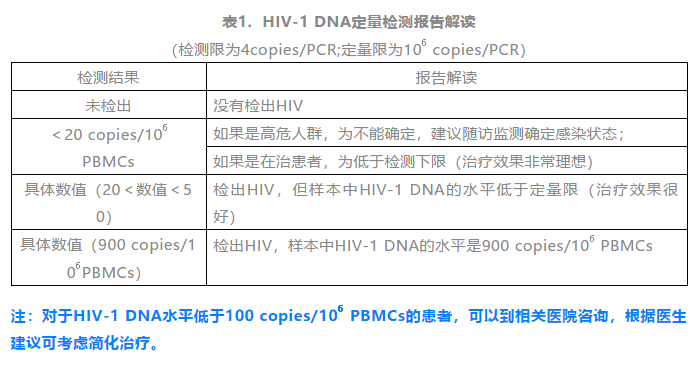
今年,北京大学-清华大学生命科学联合中心的邓宏魁教授成为入选《自然》年度人物的唯一一位中国学者。 《自然》杂志对他的描述是:“这位中国科学家将CRISPR基因编辑技术安全用于治疗艾滋病和白血病的临床研究”。
对抗艾滋病病毒,他已奋斗了二十多年
在人类攻克艾滋病病毒(HIV)的道路上,邓宏魁一直在努力。早在1996年,在美国进行博士后研究期间,他就发现了HIV入侵T细胞的主要辅助受体CCR5,这是艾滋病研究领域一项里程碑式的进展。
CCR5能帮助艾滋病毒HIV-1“溜”进人体,并破坏人的免疫系统。如果少了CCR5的帮助,是否能阻止HIV的入侵与肆虐呢?2007年,“柏林病人”通过接受具有CCR5突变的造血干细胞移植后,同时治愈了白血病与艾滋病,成为全球首例彻底治愈艾滋病的患者。2019年,“伦敦病人”在接受干细胞移植后病情持续缓解。这说明,修改或者敲除造血干细胞CCR5基因,很可能成为未来功能性治愈艾滋病的策略。
如采用干细胞移植,天然带有CCR5缺失的合适干细胞来源异常稀少,能否在体外人工“制造”出合适的干细胞呢?沿着这一思路,邓宏魁与解放军307医院的陈虎教授合作开始了一段艰苦的探索之路。
“基因魔剪”带来临床治疗新曙光

“基因魔剪”CRISPR-Cas9技术一出现,邓宏魁就看到了这种基因编辑技术为干细胞治疗带来的新曙光。
经过多年努力,邓宏魁和陈虎合作建立了利用CRISPR-Cas9进行人造血干细胞基因编辑的技术体系:通过一系列技术优化,实现了极低的脱靶率,并规避了引入外源DNA的风险,使基因编辑方法更加安全可靠。
在此基础上,他们开展了临床前研究,将敲除了CCR5基因的人造血干细胞移植到了艾滋病模型小鼠体内,构建了人造血干细胞CCR5基因敲除的人源化小鼠模型。在这个小鼠模型中,他们观察到,CCR5敲除的造血干细胞分化得到的T细胞对于HIV病毒的感染具有抵抗力,证明了这一全新疗法的安全性和有效性。

临床前试验的结果给予了团队开展临床探索性研究的信心。紧接着,邓宏魁与陈虎及北京佑安医院的吴昊教授团队在严格遵守伦理规范的情况下治愈艾滋病,获得了免疫匹配的捐献者的外周血造血干细胞,并用CRISPR-Cas9对其进行编辑,再将编辑后的造血干细胞移植到患有白血病和艾滋病的患者体内,希望通过模仿“柏林病人”,寻找治愈艾滋病之路。
但为了安全起见,他们在移植时混入了未经编辑的造血干细胞,因此患者体内检测到的基因编辑效率并不高,但经过CCR5基因编辑后的人造血干细胞所产生的T细胞同样表现出一定程度抵御HIV感染的能力。

经过19个月的临床观察,患者的白血病得到缓解,而且基因编辑效果在血液细胞中始终稳定存在,未发现基因编辑造成的脱靶及其他副作用。这初步证明了基因编辑造血干细胞在临床应用中的可行性与安全性,将促进和推动该技术在临床上的应用。
邓宏魁希望开发出将体细胞重编程为多能干细胞的方法,因为多能干细胞更易于编辑,若将其转化为造血干细胞进行移植,就有望实现100%的敲除效率。
从“一小步”积累到“一大步”跨越
多年前,邓宏魁在北京大学生命科学学院干细胞和再生生物学实验室里,悬挂过一张阿姆斯特朗在月球表面踩下第一个人类脚印的照片。
“这是我的一小步,却是人类的一大步。”邓宏魁希望学生记住这句名言:每天坚持不懈的努力,就是为了能在自己的领域里走出推动人类发展的那一小步。

2013年5月,邓宏魁课题组在美国《细胞》杂志上发表论文,发现促进分化的关键基因可以替代多潜能性关键基因,实现体细胞重编程,并由此与合作者汤超提出细胞命运决定的“跷跷板模型”,为研究细胞命运决定提供了全新视角。同年7月,他又在美国《科学》杂志上发表论文,首次实现完全使用小分子化合物逆转“发育时钟”,让小鼠体细胞重新获得多潜能性,开创了全新的体细胞重编程体系。
这一系列发现,就是邓宏魁带领研究团队积累的无数个“一小步”。这也是科学家通过干细胞技术制备精准编辑过的造血干细胞治愈艾滋病,为艾滋病患者找到新的治愈之路的科研梦想。
/uploads/",@me) /}